28 сентября 2025 Турнир Ломоносова по химии 8, 9, 10, 11 класс ответы и задания олимпиады
Решили все задания для 8, 9, 10, 11 класса XLVIII турнир Ломоносова по химии правильные ответы и решение для 48 олимпиады школьников 2025-2026 учебный год дата проведения 28 сентября 2025 начало олимпиады в 7:00 по московскому времени.
Турнир Ломоносова по химии 2025
1. Установите соответствие между различными веществами, использующимися в быту, с их химическими формулами. Обратите внимание на то, что в списке есть лишние формулы.

Ответ: Поваренная соль — NaCl, Уксусная кислота — CH3COOH, Сода пищевая — NaHCO3, Лимонная кислота — C6H8O7, Кальцинированная сода — Na2CO3.
2 задание
Установите соответствие между данными определениями и словами на тему химической промышленности, спрятанными в филворде 12×12. Слова могут читаться как слева-направо, сверху-вниз, так и справа-налево, снизу-вверх и пересекаться между собой.
Класс химических соединений, обычно состоящих из атомов водорода и кислородсодержащего или некислородсодержащего остатков. Некоторые представители этого класса используются для производства удобрений, красок и аккумуляторов.
Ответ: Кислоты
Основание, хорошо растворяющееся в воде и мылкое на ощупь. Широко используется для производства мыла, бумаги и чистящих средств.
Ответ: Щелочь
Вещество, которое вносят в почву для увеличения её плодородия и получения высокого урожая. Часто содержит азот, фосфор и калий.
Ответ: Удобрения
Материал, получаемый химическим путём из продуктов переработки нефти, газа или угля. Легкий, прочный и широко применяется для изготовления упаковок и бытовых товаров.
Ответ: пластик
Тонкая, прочная нить, получаемая химическим способом. Используется для изготовления тканей, верёвок и нетканых материалов. Пример — капрон.
Ответ: Химические волокна
«Прозрачный, хрупкий материал, получаемый сплавлением песка (оксида кремния), соды и извести. Используется для изготовления окон, посуды и бутылок.
Ответ: стекло
Большой герметичный аппарат, в котором при определенных температуре и давлении проводятся химические реакции для получения новых веществ.
Ответ: Автоклав
Вещество, которое ускоряет химическую реакцию, но само при этом не расходуется.
Ответ: Катализатор
Процесс получения сложных химических соединений из более простых.
Ответ: Химический синтез
Природные материалы, которые используются для химического производства. Например, нефть, газ, воздух, вода, минералы.
Ответ: Природное химическое сырьё
3 задание
В руки юному химику Искандеру попал старинный слиток металла, якобы серебряный, с возможной примесью олова. Прямой химический анализ может повредить артефакт, поэтому для предварительной проверки был выбран метод, известный еще со времен Архимеда. Для начала Искандер взвесил сам слиток на пружинных весах, его масса составила 2445 грамм. Затем Искандер аккуратно погрузил слиток, подвешенный на тех же весах, в тару с дистиллированной водой. Показание весов составило 2200 грамм. Справка: плотность чистого серебра – 10,5 г/см3 , плотность чистого олова – 7,3 г/см3 .
1. Определите среднюю плотность слитка (г/см3 ), основываясь на данных, полученных из опыта. Ответ приведите с точностью до сотых.
Ответ: средняя плотность слитка составляет 9,98 г/см³.
2. Определите массовые доли металлов в сплаве. Ответ укажите в процентах, с точностью до десятых.
Ответ: в сплаве содержится 75,0% серебра и 25,0% олова.
4 задание
Бесцветный газ X на протяжении десятилетий считался вредным для организма человека, однако в конце прошлого века исследователи неожиданно установили, что он участвует в регуляции важнейших физиологических процессов нервной системы. Это открытие было удостоено Нобелевской премии и стало стимулом развития ингаляционных методов терапии прекапиллярной легочной гипертензии, ишемического инсульта и других заболеваний. Ранее X производили на специальных станциях окислением газа А, имеющего плотность 0,759 г/л при н.у., кислородом на платино-родиевых сетках, заправляли его в баллоны и развозили по больницам, что было долго и дорого.
Российские ученые упростили процесс и разработали первый в мире аппарат синтеза Х для ингаляций прямо у кровати пациента путем взаимодействия двух основных компонентов воздуха в импульсно-периодическом разряде. В воздушной среде Х легко превращается в токсичный газ B, который при взаимодействии с влагой в легких образует слабую кислоту С и сильную кислоту D. Для предотвращения этого газовый поток после генератора пропускают через картридж с гидроксидом кальция, что сопровождается образованием солей кислот С и D – E и F соответственно. Примесные концентрации B в выходящем потоке необходимо тщательно контролировать. 1. Приведите формулы и названия веществ X, A-F.
2. Предельно допустимая концентрация для газа X составляет 5 мг/м3 . Рассчитайте максимальное количество молекул X, которое может содержать 1 л воздуха в помещении для терапии. Ответ представьте в стандартном виде записи числа вида a⋅10n (например, 3,4⋅104 ). В ответ запишите значения чисел a и n с точностью до целых.
3. Какой максимальный объем газа B (при 25°С и атмосферном давлении) может связать картридж, содержащий 5,0 г гидроксида кальция? Ответ укажите в л, округлите до десятых.
5 задание
Медная обшивка Статуи Свободы имеет массу 62 000 фунтов (1 фунт ≈ 0,45 кг). За 130 лет стояния в заливе Нью-Йорка на поверхности образовался слой патины. Рентгеноструктурный анализ показывает, что его основная часть – это малахит (Cu2CO3(OH)2 ). Специалисты считают, что в патину перешло около 4% от первоначальной массы меди. Схема образования малахита из меди выглядит следующим образом: Cu+CO2+O2+H2O→Cu2CO3(OH)2 Запишите уравнение реакции образования малахита. В ответе приведите сумму минимально возможных целочисленных коэффициентов.
Рассчитайте, на сколько килограммов увеличилась масса статуи за счёт образования патины. Ответ округлите до целых. В наше время периодически возникают общественные инициативы с целью «вернуть Леди Свободе её первоначальный, сияющий медный облик». Одним из предлагаемых методов является химическая очистка, которая позволила бы удалить патину, не повреждая основной металл.
Предположим, что для очистки будет использован метод обработки поверхности раствором соляной кислоты, которая реагирует с малахитом и не реагирует с медью. Рассчитайте, какой объём (в литрах) 15%-ной соляной кислоты (плотность 1,074 г/мл) потребуется для реакции со всем малахитом, образовавшимся из указанного количества меди. Ответ округлите до целых.
6 задание
Любопытному первокурснику Максиму поручили разобрать старые реактивы. На глаза ему попалась коробочка со стертой этикеткой и виднеющейся надписью «ЯД!». Внутри была баночка с металлом M под слоем парафинового масла. Юный химик заинтересовался и решил установить, какой это металл. Максим попробовал надрезать металл и обнаружил, что на воздухе он быстро покрывается блестящей пленкой (из-за образования оксида A). Далее юный химик растворил кусочек металла в разбавленной серной кислоте (с образованием соли B) и к полученному раствору наугад добавил несколько капель соляной кислоты, которые, на удивление Максима, привели к выпадению осадка (соль C).
Максим решил, что установил металл, и, чтобы подтвердить свою догадку, посветил на осадок ультрафиолетовой лампой и обнаружил изменение цвета. Подзабыв химию элементов, он вскрикнул: «Точно, это же металл X! Дает осадок в присутствии соляной кислоты, а сам осадок разлагается! Может забрать его домой?». Выходя из лаборатории с баночкой металла, Максим попался на глаза научному руководителю Виктору. «Что это ты несешь? Почему не подписано? Покажи, что внутри» – произнес его шеф. Юный бедолага вскрыл банку, и у научного руководителя чуть не встали волосы дыбом, он произнес: «Похоже я знаю, что это за металл, это Y». Чтобы подтвердить свою догадку, он взял немного металла M и аккуратно окислил его на воздухе при нагревании.
Затем растворил полученный оксид в воде и наблюдал экзотермическое растворение с образованием D. При помещении в раствор лакмусовая бумажка окрасилась в темно-синий. «Интересно, вроде и сходится, но, если это был бы супероксид E (45,01 % кислорода по массе), образованный Y, то при растворении в воде должен был бы еще выделяться и кислород» – произнес научный руководитель Максима. Тем не менее, он расспросил своего подопечного о его экспериментах, и ситуация прояснилась: «Да, это точно не Y и даже не X».
Исследователь решил для проверки окислить M озоном до оксида F (10,51% кислорода по массе). При действии на получившееся соединение концентрированной соляной кислотой выделялся газ с резким запахом. «Видишь, это металл M, он ядовит и в данном случае проявляет необычную стабильную степень окисления для своей группы. Максим, я пожалуй сам тут уберусь, а ты готовься к экзамену по химии элементов» – произнес научный руководитель юного химика. Установите формулы веществ M, X, Y, A-F.
7 задание
Несмотря на развитие альтернативных видов электрогенерации, более половины всей вырабатываемой человечеством энергии производится сжиганием различных видов топлива на теплоэлектростанциях. Сначала использовали древесину (в основном состоящую из целлюлозы), но её низкая теплотворная способность и необходимость в огромных объемах для хранения сделали дрова неподходящими для современных нужд. Другое старое топливо – уголь – оказалось удобнее и до сих пор остаётся востребованным, однако его использование сокращается для уменьшения выбросов углекислого газа.
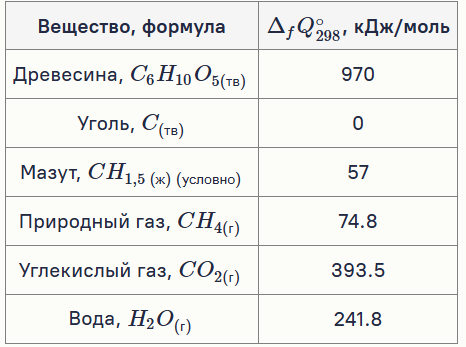
С середины XX века в ход пошёл мазут — жидкое топливо с высоким тепловыделением, но зависимость от цен на нефть и экологические проблемы препятствуют его распространению. Сегодня многие ТЭС работают на природном газе: он удобен в транспортировке, экологичнее и состоит преимущественно из метана. Ниже дана таблица с данными о наиболее часто используемых видах сгораемого топлива, а также об углекислом газе и воде. 1. Рассчитайте удельные теплоты сгорания (кДж/кг) для каждого вида топлива. Ответ округлите до целых. 2. Рассчитайте стоимости топлива за МДж энергии (руб/МДж). 3. В XX веке широкое распространение получили атомные электростанции (АЭС), где в качестве топлива используется изотоп урана — уран-235. Необходимо определить, какой массе дров в теории эквивалентен 1 грамм 235U , если при делении одного атома выделяется энергия 3,204⋅10−11 Дж. КПД считайте равным 100%. Ответ дайте в тоннах, с точностью до десятых.
8 задание
В 2023 году в эксплуатацию успешно была введена первая в мире коммерческая солнечная электростанция на основе гибридных органо-неорганических перовскитов. Эти материалы продемонстрировали феноменальную эффективность преобразования света, но их главный недостаток — быстрая деградация под воздействием влаги. Перовскиты — соединения, состав которых можно описать общей формулой ABC3 , в которой A и B — катионы металлов, C — общий анион. Также выделяют двойные перовскиты A2 BC6 . Первым хорошо изученным соединением такой структуры стал открытый в 1839 году минерал, основу которого составляет титанат кальция. Запишите его формулу.
Образование устойчивых перовскитных структур возможно комбинированием большого числа различных ионов. Это позволяет синтезировать кристаллы перовскита с широким спектром физико-химических свойств. Сегодня их находят в светодиодах, фотодетекторах, рентгеновских сцинилляторах, а теперь ещё и в солнечных батареях. Перовскитные солнечные панели стали новейшим классом плёночных солнечных элементов.
Одним из основных компонентов для таких плёнок стали синтезировать и использовать вещество W. Для синтеза 1,994 г. вещества W было взято 0,513 г. иодида метиламмония (CH3NH3I ) и 1,487 г. жёлтых кристаллов вещества X. Вещества растворили в 2 мл N,N -диметилформамида и перемешивали в течение 12 часов при температуре 60℃ в атмосфере аргона. Считая протекающую реакцию количественной, определите формулы веществ W и X. Формула W: Формула X:
Для увеличения устойчивости перовскитов к влаги было проведено несколько успешных синтезов, один из которых — двойного перовскита Y. Мотивация его получения была основана на предположении о том, что если частично заместить галогенид-анионы на другой лиганд, это должно резко повысить стабильность соединения. Для этой цели были использованы только хлорид олова (IV) SnCl4 и формиат метиламмония CH3NH3COOH . Какое окружение атома олова ожидается в Y? Выберите один вариант из предложенных:
- Линейное
- Плоскоквадратное
- Тетраэдрическое
- Октаэдрическое
Определите брутто-формулу перовскита Y, если он содержит 3,37 % водорода по массе.
Сколько атомов галогена входит в координационную сферу олова в Y?
Сколько лигандов, содеращих кислород, входит в координационную сферу олова в Y?
Синтезированное соединение Y показало необычно высокую устойчивость к влаге. Предложите структурное объяснение этого факта. Выберите один вариант из предложенных: Повышенная ковалентность связи Sn-O по сравнению со связью Sn-Cl, делает структуру более прочной и менее чувствительной к гидролизу. Осуществляется образование гидрофобного «барьера» из органических фрагментов катионов метиламмония и формиат-лигандов, который экранирует нестабильное неорганическое ядро от атаки молекулами воды. Частичное замещение хлора на крупные формиат-ионы мешает процессу внедрения молекул воды в кристаллическую решётку. В окружении атома олова в полученном перовските нет молекул воды, что наглядно демонстрирует его устойчивость к гидролизу.
9 задание
Во времена Второй Эпохи гномы Мории добывали кальциевый минерал B элемента X, известного как «Светоносный», из глубин Мглистых гор. Спеканием B, содержащего 19,97 % Х по массе, с песками Серой Пустоши и коксом из древесного угля Лотлориэна получают реакционноспособное простое вещество A. Интересно, что при растворении A в едком кали при кипячении выделяется реакционноспособный газ C и образуется соль D.
Газ С болотные эльфы прозвали «Призрачный огонь» из-за резкого орочьего запаха. Хоть и этот газ не самовоспламеняется на воздухе, его ближайший гомолог C1 способен вспыхивать сам по себе. Древние жители болот называли это явление «блуждающие огни». Методом обнаружения газа C является продувание пробы через трубку с силикагелем, на который нанесен нитрат серебра. Почернение силикагеля указывает на наличие газа C. Интересно, что в дополнении к описанным окислительным свойствам, C способен проявлять основные свойства.
В частности, образует достаточно устойчивое соединение E в реакции с иодоводородным туманом. C также может обладать восстановительными свойствами. Например, при окислении его пероксидом водорода в концентрированном растворе гидроксида натрия можно получить среднюю соль F с нехарактерной для X степенью окисления. Древняя схема, которую хранили в книгах гномов, со строением аниона в соли F, представлена на рисунке 2. Установите название элемента X, формулы веществ A, B, C, C1 , D, E, F. В ответе укажите молярные массы соединений с точностью до целых.
10 задание
Октановое число – важный показатель, характеризующий качество бензина, отображающий его стойкость к детонации при сжатии и определяющий возможность использования в двигателях различного типа. Обычный прямогонный бензин, выделяемый в ходе ректификации нефти, для использования в современных двигателях не подходит, поскольку обладает слишком низким октановым числом. Поэтому актуальной задачей является разработка высокооктановых топлив.
В начале XX века, помимо продуктов нефтепереработки, популярным топливом благодаря дешевизне и практичности стало органическое соединение A. В США A получило название «farm fuel», так как применялось для сельскохозяйственной техники и было легкодоступным вследствие наличия сырья – зерна и сахара. Во время Первой мировой войны распространение получили углеводороды одного класса B, B1 и B2, как в качестве самостоятельного топлива, так и в качестве присадки к прямогонному бензину. Промышленным методом получения B-B2 было коксование угля.
В лаборатории же B можно получить тримеризацией ацетилена над активированным углем при температуре 600oC . Смесь ближайших гомологов B1 и B2 образуется при взаимодействии метилхлорида на B в присутствии бромида железа. Интересно, что при большем количестве метилхлорида, преобладающим продуктом становится B2.
В 1921 г. Томас Миджли и его команда из General Motors обнаружили изумительные антидетонационные свойства металлорганического соединения C, содержащего 64,07 % по массе элемента Х, и началось его массовое использование в качестве октаноповышающей присадки. C получали действием насыщенного алкилхлорида D, содержащего 64,07 % хлора, на сплав натрия и металла X. Впоследствии исследователи обнаружили очень высокую концентрацию X в различных средах окружающей среды: воздухе, воде и даже в антарктических снегах. Между тем, этот металл, как оказалось, является ядовитым и не выводится организмом, поэтому применение С было сокращено.
Позднее было разработано новое октаноповышающее вещество E, основным способом получения которого является взаимодействие метанола и изобутилена в присутствии кислотного катализатора. Для получения высокооктанового компонента моторных топлив широкое распространение получил процесс алкилирования, в ходе которого углеводороды изобутан и бут-1-ен бутан-бутиленовой фракции вводят во взаимодействие с кислотным катализатором (концентрированной серной или плавиковой кислотой). Продуктом данной реакции является вещество F. 1. Укажите молярные массы веществ A, B-B2 , C, D, E, F, а также название металла X. Ответы округлите до целых.
11 задание
Соединения А, Б и В включают по три элемента, причем два элемента присутствуют в каждом из них. Примечательно, что А, Б и В имеют одинаковую стехиометрию (одинаковое соотношение атомов), но отличаются по качественному составу. Газ А во влажном воздухе частично гидролизуется, при этом образуется смесь газов с плотностью по воздуху 1,345, состоящая из веществ Д и З. При пропускании смеси в воду раствор становится кислым, причем Д образует слабую кислоту, а З – сильную кислоту.
Б можно получить взаимодействием газа Г с веществом А или бинарным соединением И, содержащим 14,9 % фосфора по массе, по следующим реакциям: 1Г + 1А → 1Б + 1Д; 1Г + 1И → 1Б + 1Е. Вещество В может быть получено реакцией бесцветной дымящей на воздухе жидкости Ж, состоящей из двух элементов, с парами воды. Известно, что в состав В входит 3d-металл в электронной конфигурации, не содержащей неспаренных электронов. Определите вещества А-И. В ответе укажите молярные массы соответствующих веществ (г/моль) с точностью до целых.

Олимпиада включает в себя соревнования по восьми предметам: астрономии, биологии, истории, лингвистике, литературе, математике, физике и химии. Вы сможете познакомиться с заданиями по всем предметам и выбрать два-три наиболее интересных для вас, чтобы погрузиться в их решение.
Смотрите на сайте
